Aldehida: struktur, sifat, tata nama, kegunaan, dan contoh
Aldehida adalah senyawa organik yang memiliki rumus umum RCHO. R mewakili rantai alifatik atau aromatik; C menjadi karbon; Atau oksigen dan H menjadi hidrogen. Mereka ditandai dengan memiliki gugus karbonil serta keton dan asam karboksilat, sehingga aldehida juga disebut senyawa karbonil.
Gugus karbonil memberikan aldehida banyak sifatnya. Mereka adalah senyawa yang mudah teroksidasi dan sangat reaktif terhadap penambahan nukleofilik. Ikatan rangkap dari gugus karbonil (C = O) memiliki dua atom yang memiliki perbedaan dalam aviditasnya untuk elektron (elektronegativitas).
Oksigen menarik elektron lebih kuat daripada karbon, sehingga awan elektronik bergerak ke arahnya sehingga membuat ikatan rangkap antara karbon dan oksigen, dengan momen dipol penting. Ini membuat senyawa aldehid polar.
Polaritas aldehid akan mempengaruhi sifat fisiknya. Titik didih dan kelarutan aldehida dalam air lebih besar daripada senyawa kimia non-polar dengan berat molekul yang sama, seperti halnya hidrokarbon.
Aldehida dengan atom karbon kurang dari lima larut dalam air, karena ikatan hidrogen terbentuk antara oksigen dari gugus karbonil dan molekul air. Namun, meningkatkan jumlah karbon dari rantai hidrokarbon menghasilkan peningkatan bagian non-polar dari aldehida, sehingga kurang larut dalam air.
Tapi, bagaimana mereka dan dari mana mereka berasal? Walaupun sifat dasarnya tergantung pada gugus karbonil, sisa struktur molekul juga berkontribusi banyak pada keseluruhan. Dengan demikian, mereka dapat dari berbagai ukuran, kecil atau besar, atau bahkan makromolekul dapat memiliki daerah di mana karakter aldehida mendominasi.
Jadi, seperti halnya dengan semua senyawa kimia, ada aldehida yang "menyenangkan" dan yang pahit lainnya. Mereka dapat ditemukan dalam sumber alami atau disintesis pada skala besar. Contoh-contoh aldehida adalah vanilin, sangat hadir dalam es krim (gambar atas) dan asetaldehida, yang menambah rasa pada minuman beralkohol.
Struktur kimia

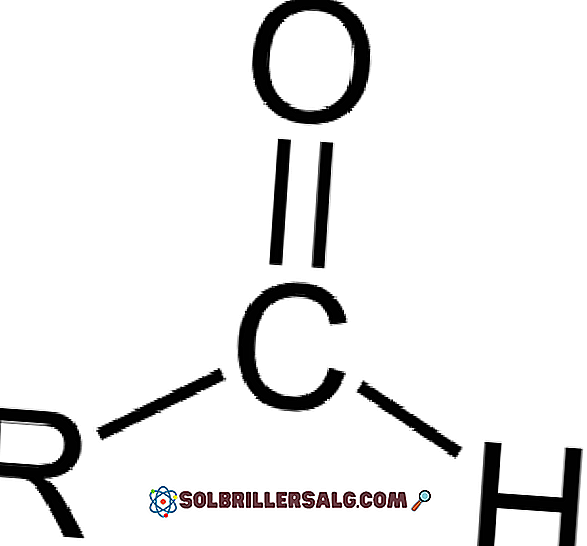
Aldehida terdiri dari karbonil (C = O) dimana atom hidrogen terhubung langsung. Ini membedakannya dari senyawa organik lain seperti keton (R 2 C = O) dan asam karboksilat (RCOOH).
Struktur molekul di sekitar -CHO, gugus formil ditunjukkan pada gambar atas. Gugus formil datar karena karbon dan oksigen memiliki hibridisasi sp2. Planaritas ini membuatnya rentan terhadap serangan spesies nukleofilik, dan karenanya mudah teroksidasi.
Apa yang dimaksud dengan oksidasi ini? Untuk pembentukan ikatan dengan atom lain lebih elektronegatif daripada karbon; dan untuk kasus aldehida itu adalah oksigen. Jadi, aldehida dioksidasi menjadi asam karboksilat, -COOH. Bagaimana jika aldehida berkurang? Alkohol primer, ROH, akan dibentuk sebagai gantinya.
Aldehida hanya diproduksi dari alkohol primer: yang mengandung gugus OH di ujung rantai. Demikian pula, gugus formil selalu di ujung rantai atau menonjol dari itu atau cincin sebagai substituen (jika ada kelompok lain yang lebih penting, seperti -COOH).
Sifat fisik dan kimia
Sebagai senyawa polar, titik leburnya lebih tinggi daripada senyawa non-polar. Molekul aldehida tidak dapat mengikat antar molekul melalui ikatan hidrogen, karena mereka hanya memiliki atom karbon yang terikat pada atom hidrogen.
Karena hal di atas, aldehida memiliki titik didih yang lebih rendah daripada alkohol dan asam karboksilat.
Titik lebur
Formaldehyde -92; Asetaldehida -121; Propionaldehyde -81; n- Butyraldehyde -99; n-Valeraldehyde -91; Caproaldehyde -; Heptaldehyde - 42; Phenylacetaldehyde -; Benzaldehyde -26.
Titik didih
Formaldehyde -21; Asetaldehida 20; Propionaldehyde 49; n-Butyraldehyde 76; n-Valeraldehida 103; Caproaldehyde 131; Heptaldehyde 155; Phenylacetaldehyde 194; Benzaldehyde 178
Kelarutan dalam air dinyatakan dalam g / 100 g H 2 O
Formaldehyde, sangat larut; Asetaldehida, tak terbatas; Propionaldehyde, 16; n-Butyraldehyde, 7; n-Valeraldehida, sedikit larut; caproaldehyde, sedikit larut; Phenylacetaldehyde sedikit larut; Benzaldehyde, 0, 3.
Titik didih aldehida cenderung meningkat secara langsung dengan berat molekul. Sebaliknya ada kecenderungan untuk menurunkan kelarutan aldehida dalam air karena berat molekulnya meningkat. Ini tercermin dalam konstanta fisik aldehida yang disebutkan di atas.
Reaktivitas
Reaksi oksidasi
Aldehida dapat dioksidasi menjadi asam karboksilat yang sesuai dengan adanya salah satu dari senyawa ini: Ag (NH 3 ) 2, KMnO 4 atau K 2 Cr 2 O 7 .
Pengurangan alkohol
Mereka dapat dihidrogenasi dengan bantuan katalis nikel, platinum atau paladium. Dengan demikian, C = O ditransformasikan menjadi C-OH.
Pengurangan menjadi Hidrokarbon
Di hadapan Zn (Hg), HCl pekat atau dalam NH 2 NH 2 aldehida kehilangan gugus karbonil dan menjadi hidrokarbon.
Penambahan Nukleofilik
Ada beberapa senyawa yang ditambahkan ke gugus karbonil, di antaranya adalah: pereaksi Grignard, sianida, turunan amonia dan alkohol.
Nomenklatur
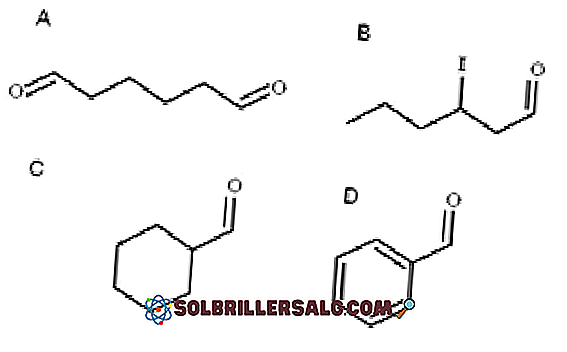
Pada gambar atas empat aldehida diilustrasikan. Bagaimana namanya?
Mengingat bahwa mereka adalah alkohol primer teroksidasi, nama alkohol diubah menjadi -ol oleh -al. Jadi, metanol (CH 3 OH) jika dioksidasi menjadi CH 3 CHO disebut methanal (formaldehyde); CH 3 CH 2 CHO ethanal (asetaldehida); CH 3 CH 2 CH 2 CHO propanal dan CH 3 CH 2 CH 2 CH 2 CHO butanal.
Semua aldehida yang baru dinamai memiliki gugus -CHO di ujung rantai. Ketika berada di kedua ujungnya, seperti pada A, pada akhir -al ditambahkan di- awalan. Karena A memiliki enam karbon (menghitung yang dari kedua kelompok formil), A berasal dari 1-heksanol dan karena itu namanya adalah: dial heksana.
Ketika ada substituen, seperti radikal alkil, ikatan rangkap atau rangkap tiga, atau halogen, karbon dari rantai utama terdaftar dengan memberikan -CHO nomor 1. Dengan demikian, aldehida B disebut: 3-iodohexanal.
Namun, dalam aldehida C dan D, gugus -CHO tidak memiliki prioritas untuk mengidentifikasi senyawa tersebut dari yang lain. C adalah sikloalkana, sedangkan D adalah benzena, keduanya dengan salah satu H mereka digantikan oleh gugus formil.
Di dalamnya, karena struktur utamanya adalah siklik, gugus formil disebut karbaldehida. Jadi, C adalah cyclohexanecarbaldehyde, dan D adalah benzenecarbaldehyde (lebih dikenal sebagai benzaldehyde).
Penggunaan
Ada aldehida di alam yang mampu memberikan rasa yang menyenangkan, seperti halnya cinnamaldehyde, yang bertanggung jawab untuk rasa khas kayu manis. Itulah sebabnya mereka sering digunakan sebagai perasa buatan dalam banyak produk seperti permen atau makanan.
Formaldehida
Formaldehyde adalah aldehyde yang diproduksi secara industri dalam jumlah yang lebih besar. Formaldehida yang diperoleh dari oksidasi metanol digunakan dalam larutan 37% gas dalam air, dengan nama formalin. Ini digunakan dalam penyamakan kulit dan dalam konservasi dan pembalseman mayat.
Demikian juga, formaldehida digunakan sebagai bahan pembasmi kuman, fungisida dan insektisida untuk tanaman dan sayuran. Namun, kegunaan terbesarnya adalah kontribusi pada produksi bahan polimer. Plastik yang disebut Bakelite disintesis oleh reaksi antara formaldehida dan fenol.
Bakelite
Bakelite adalah polimer struktur tiga dimensi dengan kekerasan besar yang digunakan dalam banyak peralatan rumah tangga seperti pegangan panci, wajan, pembuat kopi, pisau, dll.
Polimer mirip dengan bakelite dibuat dari formaldehida dalam kombinasi dengan senyawa urea dan melamin. Polimer ini digunakan tidak hanya sebagai plastik, tetapi juga digunakan sebagai perekat adhesif dan bahan pelapis.
Kayu lapis
Kayu lapis adalah nama komersial dari bahan yang dibentuk oleh lembaran kayu tipis, bergabung dengan polimer yang diproduksi dari formaldehyde. Merek Formica dan Melmac diproduksi dengan partisipasi yang satu ini. Formica adalah bahan plastik yang digunakan dalam penutup furnitur.
Plastik Melmac digunakan dalam persiapan piring, gelas, gelas, dll. Formaldehida adalah bahan baku untuk sintesis senyawa metilen-difenil-diisosianat (MDI), prekursor poliuretan.
Polyurethane
Polyurethane digunakan sebagai isolasi dalam lemari es dan freezer, bantalan furnitur, kasur, pelapis, perekat, sol, dll.
Butiraldehyde
Butyraldehyde adalah prekursor utama untuk sintesis 2-ethylhexanol, yang digunakan sebagai plasticizer. Ini memiliki aroma apel yang menyenangkan yang memungkinkan penggunaannya dalam makanan sebagai penyedap.
Ini juga digunakan untuk produksi akselerator karet. Campur tangan sebagai pereaksi perantara dalam pembuatan pelarut.
Asetaldehida
Asetaldehida digunakan dalam produksi asam asetat. Tetapi fungsi asetaldehida ini telah menurun dalam hal pentingnya, karena telah digantikan oleh proses karbonilasi metanol.
Sintesis
Aldehida lain adalah prekursor oksoalkohol, yang digunakan dalam produksi deterjen. Yang disebut oksoalkohol dibuat dengan menambahkan karbon monoksida dan hidrogen ke olefin untuk mendapatkan aldehida. Dan akhirnya aldehida dihidrogenasi untuk mendapatkan alkohol.
Beberapa aldehida digunakan dalam pembuatan parfum, seperti halnya Chanel No. 5. Banyak aldehida yang berasal dari alam memiliki bau yang menyenangkan, misalnya: heptanal memiliki bau rumput hijau; oktober sebuah aroma oranye; yang nonanal aroma mawar dan citral aroma jeruk nipis.
Contoh aldehida
Glutaraldehyde
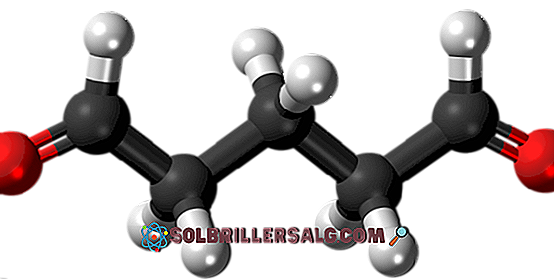
Glutaraldehid memiliki struktur dalam dua kelompok formil di kedua ujungnya.
Dipasarkan dengan nama Cidex atau Glutaral, digunakan sebagai desinfektan untuk mensterilkan instrumen bedah. Ini digunakan dalam pengobatan kutil pada kaki, mengoleskan dirinya sebagai cairan. Ini juga digunakan sebagai agen fiksatif jaringan di laboratorium histologi dan patologi.
Benzaldehyde
Ini adalah aldehida aromatik yang paling sederhana yang dibentuk oleh cincin benzen di mana gugus formil dihubungkan.
Ini ditemukan dalam minyak almond, maka bau khasnya yang memungkinkan untuk digunakan sebagai penyedap makanan. Selain itu, digunakan dalam sintesis senyawa organik yang terkait dengan pembuatan obat-obatan dan dalam pembuatan plastik.
Gliseraldehida
Ini adalah aldotriose, gula yang terdiri dari tiga atom karbon. Ini memiliki dua isomer yang disebut enantiomer D dan L. Gliseraldehida adalah monosakarida pertama yang diperoleh dalam fotosintesis selama fase gelap (siklus Calvin).
Glyceraldehyde-3-phosphate

Struktur gliseraldehida-3-fosfat diilustrasikan pada gambar atas. Bola merah di sebelah kuning sesuai dengan kelompok fosfat, sedangkan bola hitam kerangka karbon. Bola merah yang terhubung ke putih adalah kelompok OH, tetapi ketika itu terhubung ke bola hitam dan yang terakhir ke bola putih, maka itu adalah kelompok CHO.
Gliseraldehida-3-fosfat terlibat dalam glikolisis, suatu proses metabolisme di mana glukosa terdegradasi menjadi asam piruvat dengan produksi ATP, suatu cadangan energi makhluk hidup. Selain itu, dari produksi NADH, agen pereduksi biologis.
Dalam glikolisis, gliseraldehida-3-fosfat dan dihidroaseton fosfat berasal dari pembelahan D-fruktosa-1-6-bifosfat
Gliseraldehida-3-fosfat ikut campur dalam proses metabolisme yang dikenal sebagai siklus pentosa. Dalam hal ini, NADPH dihasilkan, peredam biologis penting.
11-cis-Retinal
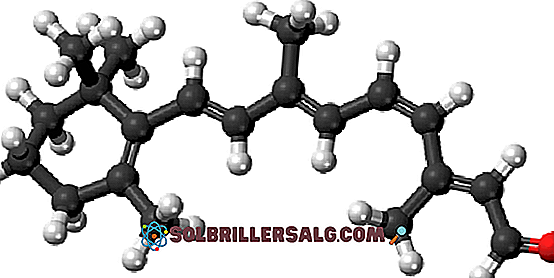
Β-karoten adalah pigmen alami yang ada di beberapa sayuran, terutama di wortel. Ia mengalami ruptur oksidatif di hati, berubah menjadi alkohol retinol atau vitamin A. Oksidasi vitamin A dan isomerisasi selanjutnya dari salah satu ikatan rangkapnya membentuk aldehida 11-cis-retina.
Pyridoxal phosphate (Vitamin B6)
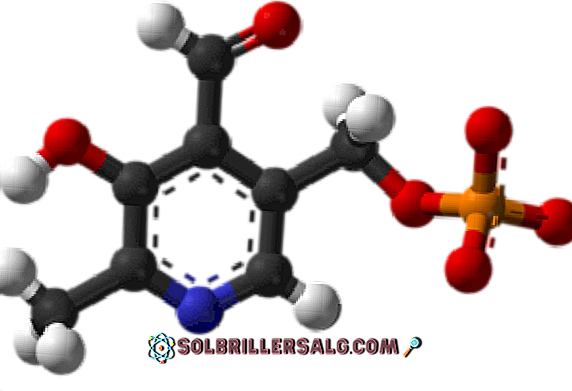
Ini adalah kelompok prostetik yang terkait dengan beberapa enzim, yang merupakan bentuk aktif vitamin B6 dan berpartisipasi dalam proses sintesis neurotransmitter GABA penghambat.
Di mana kelompok formil dalam strukturnya? Perhatikan bahwa ini berbeda dari grup yang terhubung ke cincin aromatik.
Salicylaldehyde
Ini adalah bahan baku untuk sintesis asam asetilsalisilat, obat analgesik dan antipiretik yang dikenal sebagai Aspirin.